(재)국가신약개발재단 사업개발팀
<면역증강제의 발견>
미생물학자이자 수의학자인 Gaston Ramon은 1920년대에 면역증강제(Adjuvant)라는 단어를 처음 사용했다. Adjuvant라는 용어는 라틴어 adjurer에서 파생되었으며 도움 또는 증강의 뜻을 가진다. Gaston은 면역증강제를 ‘효과적인 면역 반응을 증가시키기 위해 원하는 항원과 혼합하여 사용되는 물질’이라고 정의했다.
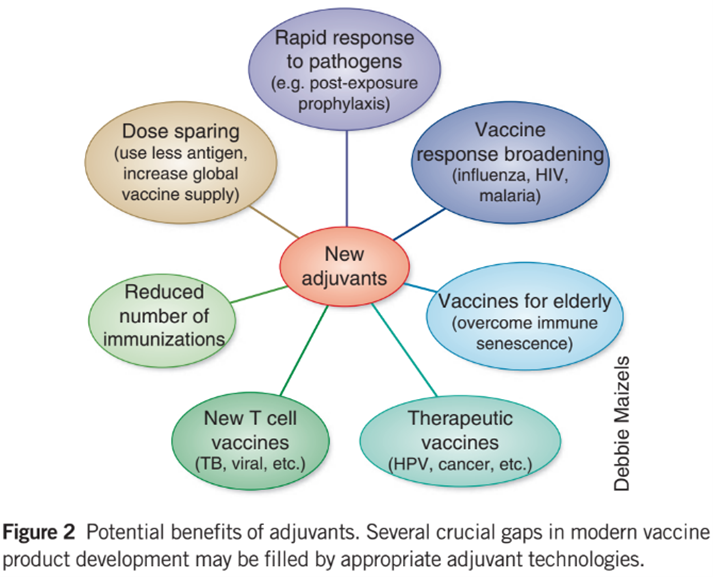
출처: Steven G Reed, Mark T Orr & Christopher B Fox. (2013). Key roles of adjuvants in modern vaccines. Nature medicine. DEC 2013
<면역증강제의 역할>
정제된 단백질 항원을 사용한 예방 접종은 일반적으로 T세포 반응이 거의 또는 전혀 없는 약한 항체 반응을 유도한다. 따라서 충분한 항체 반응을 위해서는 예방 접종을 여러 번 해야 할 수도 있다. 따라서 백신 개발자는 백신 후보물질에 면역증강제를 포함하여 약한 항원의 효능을 높여 적절한 면역 반응을 유도할 수 있다. 예를 들어, 재조합 인플루엔자 백신 후보물질이 약한 면역원성으로 인해 많은 항원양을 필요로 할 경우 백신 공급에 부정적인 영향을 미치게 될 것이다. 이때 면역증강제는 필요 항원양을 감소시켜 백신 공급을 크게 확대할 수 있다.
<면역증강제의 종류>
면역증강제는 구성요소(자연적, 인공적, 내인성), 작용기전, 그리고 물질적 및 화학적 구성에 따라 분류될 수 있다. 면역증강제는 작용기전에 따라 크게 두 범주로 나눌 수 있는데 항원 전달체(delivery system)의 역할을 하는 면역증강제, 그리고 직접 면역반응을 활성화시키는 면역증강제로 분류된다. 이와 더불어, 백신의 효능을 향상하기 위해 항원 전달체에 면역 자극 분자(immunomodulatory molecules)를 혼합한 복합 면역증강제 (Combination System)이 있다.
Delivery System 역할을 하는 면역증강제는 주로 non-immunostimulatory 입자들로 구성되어 보다 효과적인 항원 제시를 함으로써 면역반응을 유도한다고 알려졌다. 초기에 delivery system에 포함된 면역증강제들은 창고 효과(depot effect), 즉 항원을 저장하면서 천천히 제시하여 인체의 면역세포를 오랜 기간 자극해준다고만 알려졌지만, 이후 alum과 같이 몇몇 delivery system들이 내재면역을 유도할 수 있다는 점이 발견되면서 delivery system 면역증강제의 작용기전에 대한 연구가 활발히 진행되고 있다. 또 다른 종류인 면역 자극성 면역증강제 (Immunostimulatory adjuvant)는 면역 활성이 있는 물질로 이루어져서 면역세포를 직접 자극하여 내재 면역을 활성화시킴으로써 백신항원에 대한 적응 면역을 유도하는 역할을 한다. 이는 주로 TLRs, NOD-like receptors (NLRs), C-type lectins, 그리고 RIG-I-like receptors 와 같은 Pattern recognition receptors (PRRs)를 효과적으로 자극하는 agonist를 통해 백신의 면역 반응을 극대화하는 방향으로 연구되고 있다.
Delivery System은 Th2 형태의 면역 반응을 유도하는 경향이 있는데 이는 전염성 병원체에 대한 보호를 하기 충분하지 않다. 결국 충분한 보호효과를 얻기 위해서 Th1 면역과 Th2 면역을 동시에 유발하는 것이 필요하다. 항원전달체와 반대로 면역 자극성 면역증강제 (immunostimulatory adjuvant)는 Th1 면역을 포함한 선천적 면역 반응을 활성화하지만 작용기간이 그리 길지 않다. 각각 면역증강제의 이러한 단점을 극복하기 위해 작용기전이 다른 두 종류 이상의 면역증강제를 혼합한 복합 면역증강제의 개발에 주목을 하고 있다.
<현재 개발된 면역증강제의 개요 및 현황>
- Vaccine adjuvants in licensed products 

출처: O’Hagan, D. Lodaya, R. Lofano, G. (2020). The continued advance of vaccine adjuvants – ‘we can work it out’. Seminars in Immunology. 50
1) Alum
Alum은 1920년대 개발된 이래로 광범위한 백신 면역증강제로 사용되어 안전성과 효능이 입증되었다. Alum은 Depot effect를 가지고 있는 대표적인 면역증강제로서, 주로 Th2 면역반응을 일으켜 항체성 면역반응을 강화시킨다. 최근 alum의 작용기전에 대해서 분자세포생물학적 연구가 활발히 이루어지고 있는데 alum이 NLRP3 inflammasome을 활성화시켜 항체성 면역반응에 기여한다는 연구 또는 target cell에서 double-stranded DNA, uric acid, alarmin 등의 DAMPs(damage-associated molecular patterns)의 분비를 유발해 면역반응을 강화시킨다는 연구 결과가 있다. 또한 alum이 DC의 표면에 직접 반응하여 DC를 활성화시킨다는 연구 결과도 있다. 하지만 지금까지 연구 결과로는 여전히 alum의 전체적인 작용기전을 완벽하게 설명할 수 없어 이에 대한 세부적인 면역학적 연구가 활발히 진행되고 있다.
2) Oil-in-emulsion
체내에서 분해되는 oil인 squalene을 사용하여 제조된 MF59 또는 AS03과 같은 oil-in-water emulsion 면역증강제는 주로 항원성 면역반응을 강화시키고, Th1 면역반응을 보다 균형 있게 일으키는 것으로 알려져 있다. MF59는 국내 신종인플루엔자 대유행 당시에 팬데믹 인플루엔자백신의 필요 항원량을 줄이기 위해 도입되었다. 최근 연구를 통해 MF59은 alum에 비해 강한 염증반응을 일으켜 immune cell recruitment과 DC 활성화를 촉진하는 것으로 밝혀졌다. 그뿐만 아니라 follicular DC의 항원 보유를 증가시키고 TFH의 활동을 촉진하여 항체성 면역반응을 강화시킨다. 또한, 백신 접종 부위에서 DAMPs의 한 종류인 ATP의 분비를 자극하여 염증반응과 항체성 면역 반응을 촉진하는 것으로 알려졌다. AS03은 emulsion 면역증강제에 DL-α-tocopherol이 포함되어 있어, alum보다 더욱 효과적인 항체성 면역반응을 유도한다.
3) TLR(Toll-like receptor) Agonists: TLR4 agonist(AS01, AS04), TLR9 agonist(CpG)
TLR은 대표적인 PRR(Pattern recognition receptor)이며 TLR agonist가 면역세포에 대한 활성이 강하므로 면역증강제로 개발되고 있다. TLR4 agonist인 LPS는 macrophage와 DC를 자극하고, phagocytosis, MHC 발현, cytokine 분비를 촉진하여 강한 면역반응을 일으키며 Th1 항체성 및 세포성 면역반응까지 강화시키는 것으로 연구되었다. 그러나 LPS의 강한 독성으로 이를 제거한 MPL 또는 GLA가 새로운 면역증강제로서 연구되었고 복합 면역증강제인 AS04 (alum+MPL)의 주요 성분으로 포함되었다. 또 다른 복합 면역증강제인 AS01은 liposome에 MPL과 QS-21이 혼합되어 매우 효과적인 CD8+ T cell 반응을 유도한다. TLR9 agonist인 CpG는 DC, macrophage, NK cell 및 B cell 등 다양한 면역세포를 활성화하여 내재면역과 적응면역을 모두 활성화시키며 항체성과 세포성 면역반응도 증강시킨다. TLR9 agonist로 CpG motif를 포함한 oligonucleotide가 면역증강제로 개발되고 있으며 이외에도 TLR2/6 agoinst, TLR5 agonist, TLR7 agonist, TLR8 agonist가 면역증강제로 개발되고 있다.
4) Saponin (QS-21, Matrix-M)
Saponin은 Quillaja Saponaria Molina 수피에서 유래한 triterpenoid glycoside로 세포막의 콜레스테롤과 작용하여 막을 변형시켜 항원수송을 증가시키고 면역세포로부터 cytokine 분비를 증가시킨다. 정제된 saponin fraction인 QS-21은 가용성 triterpene glycosides 혼합물로 복합 면역증강제인 AS01에 사용된다. QS-21은 그 자체로 효과적인 면역증강제이나 CpG, MPL, Titermax, MoGM-CSF와 같은 다른 보조제와 함께 사용하면 더욱 효과적인 것으로 알려져 있다. Novavax의 saponin 기반 면역증강제 Matrix-MTM은 COVID-19 백신 면역증강제로 개발 중이다.
5) Liposome
Liposome은 인지질의 이중막 구조를 가지고 있는 입자를 말하는데 독성이 강한 물질이나 생체안정성이 낮은 약물을 표적세포나 기관에 전달할 목적으로 개발되었다. Liposome은 성분과 구조가 생체막과 동일하여 독성이 없으며, 그 자체로는 면역증강활성을 지니지 않지만, 양이온성 liposome은 면역활성이 있어 면역증강제로 개발되고 있다.
2020년 1월 30일, WHO의 국제적 공중보건 비상사태 선언 이후 전 세계에서 가파르게 증가하는 코로나19 전파율을 억제하기 위해 여러 제약회사들은 백신 개발에 뛰어들었다. 현재까지 미국 FDA로부터 승인된 백신(Pfizer-BioNTech, Moderna, Johnson&Johnson)은 면역증강제가 포함이 되어있지 않지만 후기 임상시험에 돌입을 하거나 2·3상 결과를 확인한 백신들 중 면역증강제를 사용한 백신 후보물질들이 여럿 있다는 점에서 눈 여겨 볼만 하다.
- COVID-19 백신에 사용된 면역증강제의 현황
Adjuvant | APPROVED VACCINE | Collaboration | Vaccine Antigen | Stage |
Alum | A number of vaccines (e.g., tetanus and diphtheria vaccines) (1930s) | Sinovac | Chemically inactivated whole SARS-CoV-2 virus particles | Approved
|
Adimmune | Recombinant RBD Vaccine | Phase 1 | ||
AS03 – GSK | Pandemic Flu H5N1 Pandemrix® (2013) | Sanofi | Recombinant S-Protein expressed in Baculovirus | Phase 1/2
|
Medicago | Coronavirus Virus-like Particles | Phase 2/3 | ||
MF59 – Seqirus | Seasonal Influenza vaccine FLUAD® (1997) | University of Queensland | SARS-CoV-2 S-clamp vaccine | Phase 1 |
CpG 1018 – Dynavax | HBV vaccine (Heplisav-B) in adults 18 or older (2017) | Clover Biopharmaceuticals | Native like Trimeric subunit Spike protein vaccine | Phase 2/3
|
Medigen | Stable prefusion Spike protein | Phase 2 | ||
Sinovac | Chemically inactivated whole SARS-CoV-2 virus particles | Approved
| ||
Valneva | Inactivated Vaccine | Phase 1/2 | ||
Matrix-M - Novavax | Various vaccines in development | Novavax | Full length recombinant SARS CoV-2 glycoprotein nanoparticle vaccine | Phase 3 |
출처: O’Hagan, D. Lodaya, R. Lofano, G. (2020). The continued advance of vaccine adjuvants – ‘we can work it out’. Seminars in Immunology. 50
가장 주목을 받고 있으며 접종률이 가장 높을 것으로 평가되는 Pfizer-BioNTech과 Moderna 백신은 핵산백신의 일종인 mRNA백신으로 승인이 된 전례가 없는 백신 플랫폼이다. 그러나 Novavax와 같은 합성항원백신인 경우, 면역 활성이 상대적으로 적어 단독적으로 적응 면역을 유도할 수 없다. 결국 이러한 백신 플랫폼의 경우 면역 원성을 증강하거나 면역 반응의 종류나 정도를 조절하기 위해 면역증강제를 추가하는 방향으로 개발되어 왔다. 이에 따라 검증된 면역증강제 개발회사인 Dynavax, GSK, Seqirus은 이전에 승인된 면역증강제 CpG 1018, AS03, MF59의 사용을 적극 지지하며 코로나 사태를 예방할 수 있는 백신을 신속하게 개발하는데 협업이 필요하다는 입장을 보였다.
1920년대 개발된 이래 광범위한 백신 면역증강제로 사용되고 있는 물질인 Alum 또한 코로나19 백신 후보물질을 위한 면역증강제로 고려되었다. 중화항체 생성을 유도하기 위해 Alum을 Spike protein이나 RBD과 제형화하였을 때 alum만으로는 CD4+와 CD8+ T세포 반응을 이끌어내기 불충분하다는 결과가 도출되었다. 오히려 emulsion이나 TLR agonist와 같은 면역 자극 면역증강제가 세포성 또는 항체성 면역반응을 강화한다는 결과를 보여주어 alum보다 더 적절하다는 결론이 나왔다. 그러나 아직 현재까지 나온 백신 임상결과로는 어떤 adjuvant가 SARS-CoV-2를 대항하기 위한 가장 적절한 유형인지 판단이 나지 않는 상황이다.
SARS-CoV-2의 변이체의 급격한 확산에도 불구하고 역학 및 발병기전에 대해 현재까지도 연구 중에 있다. 그렇기에 안전성과 유효성이 보장된 백신의 제형 및 플랫폼 선정에는 많은 고려가 필요하다. 백신 뿐만 아니라 면역활성을 증폭할 수 있는 면역증강제의 종류를 선정하기 위해서 백신 개발에 사용되는 항체의 크기(magnitude), 친화력(affinity), 동형(isotype) 및 내구성(durability) , 항원의 종류 등을 고려해야 한다. 백신 면역 증강제는 대상 병원균에 대한 감염방어기전과 대상 백신의 항원 형태, 백신 접종대상자에 따라 달라지므로 모든 백신에 한 가지 면역증강제를 공통적으로 적용하기 보다는 백신의 다양한 측면을 고려하여 선택하는 것이 바람직할 것이다.
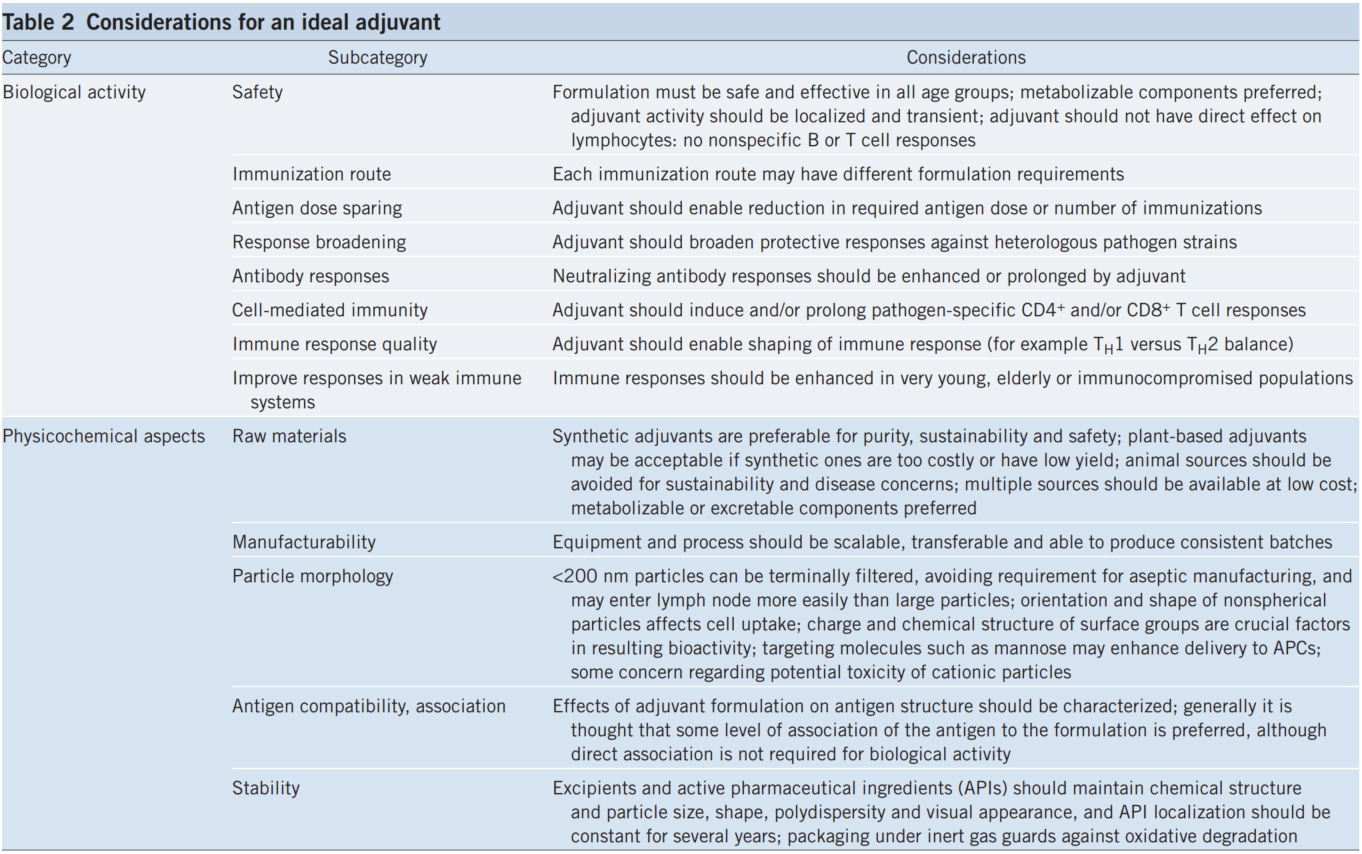
출처: Reed, S. Orr, M. Fox, C. (2013). Key roles of adjuvants in modern vaccines. Nature Medicine, 19(12).
참고자료
Awate, S., Babiuk, L. A., & Mutwiri, G. (2013). Mechanisms of action of adjuvants. Frontiers in immunology, 4, 114. https://doi.org/10.3389/fimmu.2013.00114
Didierlaurent AM, et al. (2009). AS04, an aluminum salt- and TLR4 agonist-based adjuvant system, induces a transient localized innate immune response leading to enhanced adaptive immunity. J Immunol. 183(10). 6186-97.
Getu Ayele. (2020). Review on Recent Advance of Vaccine Adjuvants. Journal of Vaccines & Vaccination. Vol. S5
Iwasaki, A. & Yang, Y. (2020). The potential danger of suboptimal antibody responses in COVID-19. Nature Review Immunology. 20, 339–341
Liang, Z. et al. (2020). Adjuvants for Coronavirus Vaccines. Front Immunol.
O’Hagan, D. Lodaya, R. Lofano, G. (2020). The continued advance of vaccine adjuvants – ‘we can work it out’. Seminars in Immunology. 50
Steven G Reed, Mark T Orr & Christopher B Fox. (2013). Key roles of adjuvants in modern vaccines. Nature medicine. DEC 2013
김의호(2018). 백신 면역증강제(vaccine adjuvant)의 개발 동향. BRIC View 2018-T03 Available from http://www.ibric.org/myboard/read.php?Board=report&id=2896
이전
2021.02.09
다음