|
(재)범부처신약개발사업단 『범부처전주기신약개발사업 사업화지원사업_신약 임상개발 컨설팅(ACT)』 사업수행자 선정 공고 |
(재)범부처신약개발사업단은 「범부처전주기신약개발사업 사업화지원사업_신약 임상개발 컨설팅(ACT)」프로그램 사업수행자 선정 공고를 아래와 같이 하오니 참여를 희망하시는 사업수행기관에서는 아래 절차 및 첨부한 제안요청서에 따라 신청하여 주시기 바랍니다.
1. 사업 개요
○ (사업명) 범부처전주기신약개발 사업화지원사업_신약 임상개발 컨설팅(ACT)프로그램
○ (사업내용)
- 국내외 임상시험 전문가, 임상시험 글로벌선도센터, 질환별 임상전문의 등 국내외 전문가로 구성된 컨설팅 지원단 운영
- 질환별 Medical Unmet Needs, 개발약물의 MOA와 물질특성을 고려한 임상시험 전략, 시장에서의 경쟁적 차별화 전략 등을 포함한
임상 시험 디자인(목표환자군 선정, 독성 및 효능검증을 위한 기준 및 바이오마커, 임상시험 PI선정 등), 최적 CRO 선정 등을 지원
- 범부처신약개발사업단 보유 파이프라인에 대한 차 상위단계 임상개발 전략 및 개발계획 컨설팅, 진행 중인 임상시험 과제의 Risk
평가 및 자문, 임상시험 디자인을 고려한 초기단계 개발전략 수립 지원 등 컨설팅 서비스 지원
○ (추진체계)
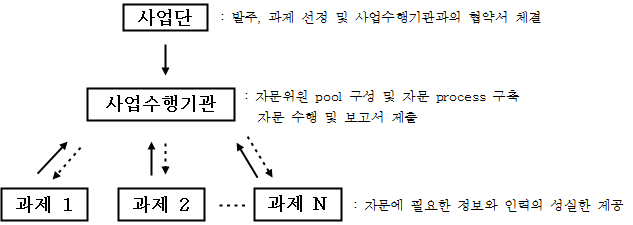
○ (계약기간)
- 총 계약기간: ‘17. 9. 1 ~ ‘19. 8. 31 (총 24개월)
1차년도: ‘17. 9. 1 ~ ‘18. 2. 28 (총 6개월)
2차년도: ‘18. 3. 1 ~ ‘19. 2. 28 (총 12개월)
3차년도: ‘19. 3. 1 ~ ‘19. 8. 31 (총 6개월)
- 당해년도 사업기간의 성과에 따라, 차년도 사업 연장이 가능
○ (사업예산)
- 총 계약기간: ‘17. 9. 1 ~ ‘19. 8. 31 (총 24개월)
- 총 600백만원 이내(VAT 포함)
- 차년도 예산은 정부 사정에 의해 변경될 수 있음
2. 사업 내용 요약
|
과제 |
범부처전주기신약개발 사업화지원사업_신약 임상개발 컨설팅(ACT) 프로그램 |
유 형 |
R&D 사업화 지원 사업 |
| 사업기간 | 총 사업기간: ’17. 9. 1. ~ ’19. 8. 31.
1차년도: ’17. 9. 1 ~ ’18. 2. 28 2차년도: ’18. 3. 1 ~ ’19. 2. 28 3차년도: ’19. 3. 1 ~ ’19. 8. 31 |
사업비 |
총 600백만원 이내 (VAT 포함) |
|
배 경 및 목 적 |
○ 2015년 기준 국내 임상이행률은 평균 7%로서 글로벌 빅파마 평균이행률 12% 대비 약 1/2 수준으로, 국내 신약개발 3대 장벽 중 하나임 ○ 효과적인 임상개발 전략 수립 및 임상시험 디자인 설계를 통해 가능하면 국내에서 후기임상시험까지 성공적으로 완료함으로 써 개발약물의 가치를 높이는 동시에, 개발기간을 최대한 단축함으로써 라이센싱 성공가능성을 증가시키기 위한 임상개발 역량을 제고할 필요가 있으나, 글로벌 수준의 혁신신약 임상개발 경험이 부족한 국내 제약기업의 현실을 고려하여 국내외 최고 수준의 임상시험 전문가, 임상전문의, 임상시험센터 등을 연계한 신약 임상개발 컨설팅 지원 사업 추진 필요 |
||
|
내 용 및 범 위 |
○ 자문위원단 구성 ○ 발주기관이 선정한 과제에 대해 임상개발계획(CDP) 및 임상시험계획서(protocol) 개발 등에 대한 자문 - 대상: 범부처전주기신약개발사업 과제로 선정된 과제 중 임상 제 1상 및 제 2상 시험 개시를 계획 중인 과제 (1차년도 3개 내외, 2차년도 5개 내외, 3차년도 3개 내외) - 자문 범위: 임상개발계획(CDP)과 프로토콜 개발 자문을 기본으로 하나 회사역량, 과제의 성격 및 예산범위 내에서 아래의 내용자문을 포함하는 것을 권장 ♦ 개발전략(Development strategy) ♦ 임상개발계획(Clinical development plan) ♦ 임상시험디자인(Clinical trial design including sample size) ♦ 임상시험계획서 컨셉(Protocol concept) ♦ 연구 발표 계획(Publication plan) ♦ 임상시험 관리 계획(project management) - 자문에 포함되지 않는 것: 개발약물 자체의 문제점, 개별국가 별 개발전략 (country-specific regulatory strategy), 통계분석계획(SAP), full protocol writing 등 - 자문형태: 대면 자문 및 서면 자문 보고서 - 성과목표: 1차년도 3개 내외, 2차년도 5개 내외, 3차년도 3개 내외 대상 과제에 대한 대면 자문 또는 서면 자문 보고서 |
||
|
기 대 효 과 |
○ 국내 신약개발 3대 장벽 중 하나인 임상이행률 제고를 통한 국내 신약개발 성공 가능성 증대 및 시장경쟁력을 가진 약물개발을 통해 라이센싱 가능성 및 가치극대화 ○ 질환별, 물질특성별 컨설팅 사례분석을 통한 글로벌 수준의 임상시험 디자인 역량 산업계 확산 |
||
3. 신청 방법
○ (접수기간) 2017. 8. 10.(목) ~ 2017. 8. 11.(금) 18시까지
○ (신청방법) 제안서 및 별도 제출서류 일체의 내용을 수록하여 이메일로 제출
- 이메일 : kddf_pm@kddf.org
- 전 화 : 02-6379-3071 (담당)
※ 이메일 접수 후 유선으로 접수 확인 요망
4. 사업 수행기관에 대한 제한
○ 선정된 사업 수행기관은 본 사업에서 컨설팅 대상이 된 과제와 관련하여 향후에 임상시험 수행등과 관련한 용역계약 등 유상 계약을 체결
하여 과업을 수행할 수 없음
첨부 : 범부처신약개발사업 사업화지원사업_신약 임상개발 컨설팅(ACT) 사업수행자 선정 공고_제안 요청서
끝.
이전
다음