[국가신약개발사업]
[공고번호 고 23-13]
글로벌 RA (Regulatory Affairs) 지원사업 접수 공고 |
국가신약개발사업단은 「글로벌 Regulatory Affairs 지원사업」을 아래와 같이 공고하오니 참여를 희망하시는 사업수행기관
에서는 아래 절차 및 첨부한 제안요청서에 따라 신청하여 주시기 바랍니다.
2023년 3월 23일
국가신약개발사업단장
1. 사업 개요
○ 사 업 명 : 글로벌 RA (Regulatory Affairs) 지원사업
○ 사업 내용 : 글로벌 RA 지원사업 운영
- 사업단 과제(7개 내외)의 글로벌 Regulatory Affairs(미국 FDA IND 등) 지원
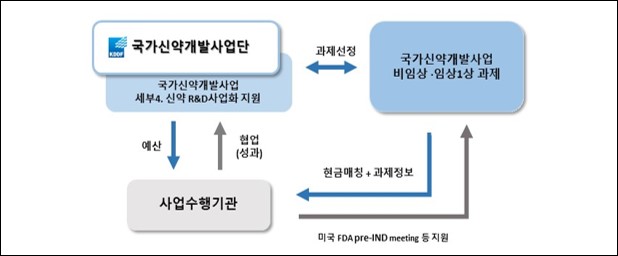
○ 추진 체계 : 국가신약개발사업단과 사업수행기관 간의 협업을 통해 추진
<글로벌 RA 지원사업 추진체계(안)>
○ 계약 기간 : '23. 5. ~ '24. 3. 31.
○ 사업 예산 : 총 오억삼천만원 (₩ 530,000,000원, 부가세 포함)
2. 사업 내용 요약
과 제 | 글로벌 RA (Regulatory Affairs) 지원사업 | 유 형 | R&D 사업화 지원 사업 |
사업 기간 | '23. 5. ~ '24. 3. 31. | 사 업 비 | 총 오억삼천만원 이내 (₩ 530,000,000원 이내, VAT 포함) |
배경 및 목적 | ○ 국가신약개발사업단에서 지원한 과제들의 성숙도가 높아지고 연구 수행주체 기관들의 해외 진출에 대한 높은 수요에도 불구하고 아직까지 일부 대기업을 제외하고 해외 진출을 위한 인력, 경험이 부족함. 따라서 해외 Regulatory Affairs를 전문적으로 지원할 필요성이 있음 ○ 사업단 과제수행기관의 글로벌 신약개발 과정 중 복잡한 인허가 절차로 인해 겪는 어려움을 최소화하기 위해 과학적 요건 충족을 위한 Regulatory 업무의 집중 지원 수요 존재 ○ 미국 FDA의 규제 및 실무에 이해도가 높은 Regulatory Affairs 전문 업체를 활용하여 미국 IND 신청 등의 지원사업을 통해 국제 제약사의 글로벌 진출을 가속화 하고자 함 ○ 국내 제약산업의 글로벌화 지원을 위한 생태계 확보 | ||
내용 및 범위 | 사업단 과제(7개 내외)의 글로벌 Regulatory Affairs(미국 FDA IND 등) 지원 ○ Pre-IND meeting - 주관연구기관 요청에 따른 미국 FDA Pre-IND meeting 업무 지원 ○ IND filing and management - 주관연구기관 요청에 따른 미국 FDA IND filing and management 업무 지원 ○ 기타 자문 - 주관연구기관 요청에 따른 미국 FDA IND filing을 위한 Gap analysis 및 early phase study의 protocol, synopsis 검토 등 자문 ○ 기타 미국 FDA IND 및 NDA 대비 사전 준비 가이드 업무 등 | ||
기대 효과 | ○ 국내 신약 연구개발 주체 기관의 해외, 특히 미국 IND 신청 경험이 풍부한 전문 업체를 통한 역량 강화 효과를 낼 수 있으며 궁극적으로는 국내 제약사의 글로벌 시장 진출을 도모하고자 함 ○ 해외 IND 경험이 풍부한 사업수행기관과 업무 추진을 통한 실무 경험 증진으로 국내 제약사 및 바이오 벤처의 역량 강화 | ||
3. 신청 방법
○ 접수 기간 : 2023. 3. 23.(목) ~ 2023. 4. 5.(수) 18시 까지
○ 신청 방법 : 제안서 및 별도 제출서류 일체의 내용을 수록하여 우편접수 (제안서 및 발표자료 원본 10부, 별도 제출 서류,
원본 USB 첨부) 및 직접 방문으로 접수
※ 마감 일시까지 우편 접수를 모두 완료하여야 함
* 접수처 : (우편번호:04143) 서울시 마포구 마포대로 137 KPX빌딩 9층 국가신약개발사업단
* 이메일 : 조민재 연구원 (rnd_project@kddf.org)
* 문의처 : 02-6379-3065 (담당)
첨부 1. 글로벌 RA (Regulatory Affairs) 지원사업 제안요청서 1부. 끝.
이전
2023.03.09
다음
2023.03.28